确保符合欧盟医疗器械法规(EU MDR)的最后期限即将到来。这些更严格的新法规旨在改善在欧盟内销售的医疗设备的可追溯性和安全管理。距离截止日期还有不到九个月的时间,医疗器械制造商已经开始倒计时,以确保它们符合要求。
担心新规定对你意味着什么吗?在这篇文章中,Volker Watzke, Domino印刷科学公司的欧盟医疗设备部门经理,提供了关于如何尽可能快速和有效地合规的建议。

概述:欧盟MDR要求什么?
欧盟MDR将于2020年5月26日生效,取代欧盟现行的医疗器械指令(93/42/EEC)和主动植入式医疗器械指令(90/385/EEC)。
作为新法规的一部分,在欧盟内销售的医疗设备制造商必须遵守严格的指导方针,以确保其产品的使用安全。这些规定涵盖了在欧盟销售的所有医疗器械——从手术刀、针头到心脏起搏器、隐形眼镜和假肢。
从2020年5月26日起,所有医疗器械将需要分配一个唯一的器械标识(UDI)代码。属于III类和IIa/b类的器械将需要在一个名为EUDAMED的欧盟中心数据库上记录、索引和注册其UDI(欧洲医疗器械数据库)。
III类和IIa/b类产品的制造商将负责根据该法规附件VI b部分共享产品数据。I类产品制造商也将被要求收集和保存产品数据,但只需要在要求时共享这些信息。
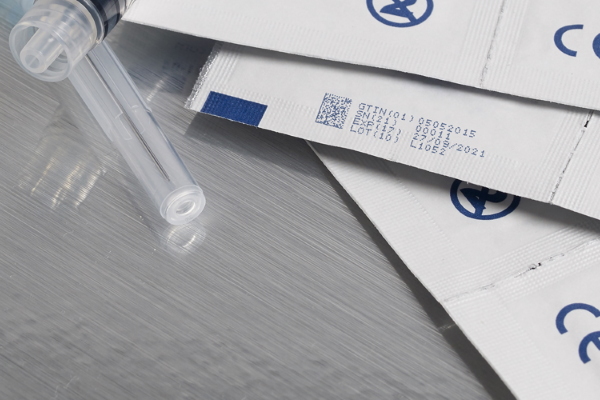
欧盟MDR的引入要求医疗器械制造商对技术进行投资,以使可追溯性编码能够在单个产品级和包装上快速和准确地应用。
不遵守这些程序可能意味着设备将从销售中撤出,设备制造商将不再能够向其他欧盟成员国供应产品。
我们现在在哪里?

医疗器械制造商应及时了解当前的发展情况,并向GS1等当局以及公告机构和可信任的合作伙伴征求意见和支持。会议、网络研讨会和活动可以提供关于如何最好地管理程序和为新规定做准备的丰富信息。
截至撰写本文时,EUDAMED的技术规范预计将于2019年底发布。迄今为止,制造商受益于欧盟委员会(European Commission)发布的技术公告,该公告提供了应如何提交数据的信息。该技术公报针对每个制造商的不同需求。
从EUDAMED技术规范发布到最终注册日期,制造商将有大约5-6个月的时间。因此,建议尽快开始收集数据。制造商需要根据欧盟MDR附录VI B部分收集每个产品的数据,并开始准备数据以便在EUDAMED上共享。
除了在2020年5月的最后期限之前准备好所有数据,制造商还应该确保他们有正确的合作伙伴在整个过程中支持他们。为了确保他们的设备符合新法规,制造商应该向他们的代码发布机构和公告机构征求意见。
目前,一些大型医疗设备制造商正在利用多达25%的员工基础,使其程序达到标准。中小型制造商不太可能有能力投入这么多劳动力,应该考虑外部支持的选择。
发行机构
2019年6月,GS1成为欧盟MDR合规代码的第一个发行机构,这意味着2D Data Matrix和GS1-128代码可以继续使用。预计其他发行机构也将效仿,将来有可能使用HIBCC和ICCBBA编码。
通知的身体
作为现行欧盟指令(90/385/EWG)和(93/42/EWG)的一部分,制造商定期对其产品进行审核和检查,以确保产品符合要求。公告机构支持制造商在此过程中确保新产品和现有产品可以销售。在整个欧洲处理当前立法的57个通报机构中,只有38个申请了欧盟MDR认证。
截至撰写本报告时,只有4个公告机构获得了新的认证。
制造商可以决定为其产品选择哪个公告机构,但应记住,一些现有的公告机构将不再根据欧盟MDR提供援助。新的认证程序更具挑战性,因此,大约有20个公告机构尚未提出申请。
突然缺乏公告机构已经成为制造商寻求产品认证的瓶颈,也可以被视为创新的障碍,因为初创企业很难找到支持。希望注册产品的初创企业应该向四个新认证的公告机构中的一个咨询。
一个全球性的影响
欧盟MDR涵盖了所有在欧盟内销售的产品,但这并不意味着只有欧盟成员国才能满足要求。所有希望在欧盟销售其产品的制造商需要确保他们满足欧盟MDR要求,否则他们的产品可能会被从销售中移除。
同样,根据欧盟MDR注册的制造商今后应将注意力集中在确保世界各地的合规上,因为这些地区可能会有额外的立法。目前,美国、印度和韩国正在通过关于医疗器械和药物识别的立法,澳大利亚、巴西、加拿大、中国、哥伦比亚、日本、新西兰、俄罗斯、沙特阿拉伯、新加坡和土耳其正在进行进一步的讨论。
谁能提供进一步的建议和支持?
随着确保遵守欧盟耐多药抗药性的最后期限迅速临近,现在是采取行动的时候了。
Domino的专家可以帮助您确保您的产品符合即将到来的EU MDR。在Domino,我们提供验证包来帮助制造商认证他们的产品并为EU MDR认证做准备。
我们的编码和标记解决方案系列为医疗设备制造商提供最合适的技术,以实现UDI合规。有关如何确保您的编码符合EU MDR的建议和支持,请与Domino的专家联系。
要进一步了解即将发布的EU MDR,请收听Domino的最新播客https://go.domino-printing.com/medicaldevicespodcast


Volker Watzke是Domino印刷科学公司的欧盟医疗设备部门经理







